Kultury in vitro (z łac. w szkle), kultury tkankowe to technologia, która umożliwia namnażanie linii komórek, tkanek, a także otrzymywanie z niezwykle wysoką wydajnością sadzonek zdrowych, silnych roślin. Produkcja takich roślin wcale nie odbywa się w szklarni, czy plantacji ale w laboratorium w sterylnych warunkach i przy pomocy odpowiedniego medium hodowlanego – pożywki, żelu. To właśnie laboratorium stanowi główny filar produkcji roślinnej na świecie. Nie chodzi tylko o rośliny akwariowe ale również ozdobne, czy drzewa i krzewy owocowe. Właśnie ta większa dostępność, również cenowa, wielu gatunków roślin akwariowych jest spowodowana upowszechnieniem technologii kultur in vitro. Technologia ta pozwala uzyskiwać sadzonki w krótszym czasie niż uprawiane konwencjonalnymi sposobami rośliny.



Historia kultur in vitro sięga początku XX wieku. W 1902 roku austriacki botanik i fizjolog roślin Gottlieb Haberlandt zaproponował stworzenie kultury komórek w sztucznych, kontrolowanych warunkach w szklanych naczyniach. Stąd in vitro, czyli w szkle. Udało mu się wyizolować pojedyncze komórki różnych gatunków roślin, a następnie zmusił je do wzrostu. Celem miało być uzyskanie podziałów tych komórek co niestety się nie udało. Mimo to Haberlandt dzięki swojej pracy i pionierskim tezom na temat czynników wpływających na kulturę komórek został nazywany ojcem kultur in vitro. Stworzył mocne podwaliny do prac dla kolejnych badaczy. Jak się później okazało wiele z jego przypuszczeń zostało potwierdzone przez innych badaczy. Podobne zainteresowanie w tych latach dotyczyło również kultur in vitro komórek zwierzęcych! Przez lata roślinne kultury in vitro były daleko w tyle za kulturami zwierzęcymi. Brakowało przełomowego odkrycia, które dałoby nowe narzędzia do pracy i popchnęło badania do przodu. Pod koniec lat 20tych XX wieku F. Went i N.G. Chołodny niezależnie od siebie udowodnili istnienie auksyn – jednej z grupy roślinnych regulatorów wzrostu lub potocznie mówiąc hormonów roślinnych. Potwierdzili i opisali oni to co sugerowano już w 18 wieku. W drugiej połowie XVIII wieku po raz pierwszy zasugerowano istnienie substancji, które przemieszczają się w roślinie i dają sygnały do pewnych działań. W 1880 Darwin badając fototropizm pewnego gatunku doszedł do wniosku, że istnieje substancja produkowana w stożku wzrostu, która wpływa na wyginanie roślin do słońca. Hormony w roślinach naturalnie występują w bardzo małych ilościach i charakteryzują się bardzo silnym działaniem. Pierwsze nieświadome użycie hormonów roślinnych przez ludzi zostało dokonane na długo przed Chrystusem. Przyśpieszenie dojrzewania figi stymulowano nakropleniem na owoc oleju z oliwy. Wtedy nie wiedziano, że z czasem pod wpływem ciepła z oliwy wydziela się etylen – hormon starzenia, który przenikając do komórek owocu figi przyśpieszał jej dojrzewanie. W 1930 zaczęto używać etylenu do przyspieszenia kwitnienia ananasa. Poszczególne grupy roślinnych regulatorów wzrostu i ich działanie zostanie opisane w dalszej części rozdziału. Odkrycie hormonów roślinnych dodało zatem naukowcom z początku dwudziestego wieku przełom w badaniach. Odkryto, że z utrzymywanej w kulturze in vitro tkanki przyrannej, czyli kallusa, można uzyskać organogenezę – wytwarzanie organów rośliny. Zaczęto także wydłużać czas w jakim kultury mogły być prowadzone. Kolejnym kamieniem milowym było opracowanie w 1962 roku przez Murashige i Skoog’a zestawienia soli mineralnych w odpowiednich proporcjach. Była to pożywka do prowadzenia kultur in vitro tytoniu. Okazała się ona jednak niezwykle skuteczna w przypadku kultur innych gatunków roślin. Obecnie używa się jej w prawie każdym laboratorium badawczym, a nazwana została od nazwisk badaczy pożywką MS. Po opracowaniu składu tej pożywki nastała era masowej produkcji roślin w laboratoriach. Rozmnażano głównie rośliny trudne w rozmnażaniu tradycyjnymi metodami, gatunki drogie jaki i te rzadkie.
Oprócz uzyskiwania sadzonek roślin kultury in vitro oferują otrzymywanie mieszańców międzygatunkowych, nowych odmian roślin, uwalnianie roślin od patogenów, a nawet kultury samych korzeni włośnikowatych, bez części zielonej rośliny! Produkowane są w ten sposób metabolity wtórne, często substancje cenne w lecznictwie.
Mikropropagacja, czyli szeroko pojęte otrzymywanie sadzonek roślin drogą kultur in vitro jest w obecnych czasach powszechnie używaną metodą klonalnego rozmnażania roślin. Prawidłowe posługiwanie się tą techniką umożliwia uzyskiwanie roślin, które są genetycznie wiernymi kopiami rośliny rodzicielskiej. Jakie rośliny chcemy ‘kopiować’? Najlepiej tylko najciekawsze osobniki z populacji. Chodzi o to, aby powielić ich wyjątkowe cechy i zaproponować akwaryście jak najlepszej jakości rośliny. Muszą to być rośliny zdrowe, charakteryzujące się odpowiednim wzrostem, interesującą kolorystyką, kształtem liścia oraz odpornością na choroby. Tą metodą można otrzymać w dość krótkim czasie ogromną liczbę klonów wybranej elitarnej rośliny. Jest to jeden z powodów, dla których rośliny w żelu stają się coraz bardziej popularne wśród akwarystów.
Aby założyć kulturę in vitro, wybraną elitarną roślinę trzeba pozbawić patogenów, a także glonów, ślimaków, czy innych organizmów znajdujących się na ich powierzchni. W tym celu należy wyciąć pewien fragment rośliny (eksplantat) i umieścić go w roztworze odkażającym. Rośliny ze względu na odmienną budowę, grubość skórki lub obecność kutykuli wymagają innego traktowania. Indywidualnie dla gatunku dobiera się więc substancję odkażającą oraz czas odkażania. Odkażać można w roztworach podchlorynu sodu, etanolu, czy wodzie utlenionej. Po odkażaniu trzeba odpłukać substancję odkażającą w sterylnej wodzie. Na ogół stosuje się trzy płukania, a następnie umieszcza eksplantat na pożywce.
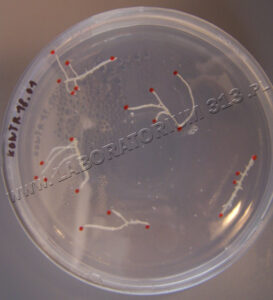
O roślinach z in vitro mówi się, że są sterylne, aseptyczne. W wielu przypadkach rzeczywiście tak jest. Trzeba jednak wiedzieć, że wiele kultur może prawidłowo wzrastać pomimo obecności w ich tkance grzybów lub bakterii. Nie znajdują się one na powierzchni eksplantatu, który został przecież powierzchniowo odkażony ale wewnątrz tkanek. Są to endobakterie i endogrzyby. Te endomikroorganizmy nie ujawniają się dopóki roślina jest silna, a jej komórki dzielą się szybko, uzyskując ogólny wzrost pędów. Jednak, gdy tkanka roślinna słabnie ponieważ zaczyna brakować jej substancji odżywczych albo zbyt długo znajduje się w kulturze, endomikroorganizmy mogą ‘wyjść’ z tkanek roślinnych. Przestają wtedy żyć w roślinie i odżywiać się z jej zasobów, a zaczynają wykorzystywać pożywkę. Jest to bardzo niebezpieczne, a w większości przypadków śmiertelne dla roślin. Są dwa główne czynniki przez które endomikroorganizmy potrafiące współżyć z rośliną stają się jej śmiertelnymi wrogami. Po pierwsze komórki mikroorganizmów dzielą się o wiele szybciej niż komórki roślin. Podziały komórkowe mikroorganizmów liczymy w minutach natomiast podziały komórek roślinnych w godzinach. Dlatego kultura in vitro roślin może zostać szybko przejęta przez niechciane mikroorganizmy. Zwyczajnie bakterie i grzyby są szybsze w kolonizowaniu środowiska i konkurencji do substancji odżywczych z żelu. Po drugie mikroorganizmy wydzielają substancje allelopatyczne do pożywki. Komórki roślinne stają się osłabione przez co nie dzielą się już tak szybko jak powinny. Bakterie i grzyby zaczynają z łatwością zarastać zarówno pożywkę jak i same rośliny. W ten sposób powstaje zakażenie mikrobiologiczne. Zakażona kultura powinna zostać zutylizowana, aby w laboratorium nie zwiększać udziału mikroorganizmów, które mogą zaatakować kolejne kultury.
Dla celów mikropropagacji można używać zarówno komórek, tkanek, czy organów. Rośliny, a właściwie komórki, z których są zbudowane posiadają ogromny potencjał regeneracyjny. Nazywamy go totipotencją. Dzięki niej nawet z pojedynczej komórki można otrzymać kompletną roślinę! To właśnie totipotencja stanowi podstawę kultur in vitro. Najprostszym sposobem na otrzymanie kultury in vitro jest użycie tkanki merystematycznej, czyli tkanki twórczej. Tkanka merystematyczna znajduje się w ściśle określonych częściach rośliny, wszędzie tam gdzie dochodzi do intensywnych podziałów komórkowych. Umieszczając eksplantat, który zawiera właśnie te komórki w żelu, możemy zainicjować powstanie rośliny potomnej, zupełnie takiej samej pod względem genetycznym jak roślina, z której zostały pobrane komórki. Różny skład żelu, który jest mieszaniną makro- i mikroelementów, hormonów, agaru oraz innych substancji może stymulować różne efekty. Może dojść do bezpośredniej regeneracji pędów z fragmentu rośliny, może powstać kallus (tkanka przyranna, taka sama jaką tworzą np. drzewa po odcięciu gałęzi) lub nawet zarodki somatyczne. Kallus jest dość ciekawą strukturą. Jest on nieuporządkowaną masą komórek, która ma zdolność do nieograniczonych podziałów. Można dzielić go na mniejsze fragmenty i znowu namnażać. Po umieszczeniu go na pożywce o innym składzie może różnicować w pędy. Metoda ta jest bardzo wydajna, ponieważ z kilkumilimetrowej grudki kallusa możliwe jest uzyskanie kilkudziesięciu pędów roślin. Te pędy po odcięciu i przeniesieniu na pożywkę ukorzeniającą gotowe są do aklimatyzacji w akwarium. Zarodek somatyczny jest zarodkiem powstałym nie z gamet, tak jak ma to miejsce w naturze podczas zapłodnienia, lecz z komórki somatycznej – wegetatywnej. Oznacza to, że w określonych warunkach z dowolnej komórki rośliny mogą tworzyć się zarodki. Im komórka, na którą się działa jest mniej wyspecjalizowana, tym łatwiej jest uzyskać zarodki somatyczne. Wszystkie wyżej wymienione procesy są sposobem rozmnażania klonalnego.



Kluczem do skutecznego rozmnażania roślin w warunkach in vitro jest odpowiedni skład żelu. To właśnie jego skład umożliwia wybór drogi rozmnażania rośliny. Można manipulować ilością regenerujących pędów, rozrostem systemu korzeniowego, szybkością podziałów kallusa, itd. Każda roślina ma inne wymagania pokarmowe. Z tego względu mieszanina soli używanych do sporządzenia pożywki jest różna dla poszczególnych rodzajów, gatunków, a nawet odmian roślin. Pomimo wielu opisanych pożywek najbardziej uniwersalną i najczęściej stosowaną pożywką jest wciąż pożywka MS (Murashige & Skoog, 1962). W skład żelu wchodzą wszystkie pierwiastki potrzebne roślinom do wzrostu w postaci soli mineralnych, łatwo przyswajalny cukier jako źródło węgla (trzeba pamiętać, że węgiel to podstawowy budulec organizmów żywych) oraz regulatory wzrostu i bardzo często substancja żelująca, która nadaje pożywce konsystencję żelu. Skoro substancja żelująca jest opcjonalna to pożywki mogą mieć różny stan skupienia. Mogą być płynne, półpłynne bądź zestalone, w zależności od potrzeb i sposobu ich użycia. Pożywki stałe są najczęściej stosowane w przemysłowej produkcji in vitro. Pożywek płynnych używa się najczęściej w mocno wyspecjalizowanych procesach np. w kulturach zawiesinowych, w bioreaktorach do kultur korzeni włośnikowatych, bądź komórek embriogenicznych. Mimo pierwotnie używanej pożywki płynnej w mocno wyspecjalizowanych kulturach coraz częściej pojawiają się w sklepach akwarystycznych rośliny z in vitro ale nie w żelu tylko właśnie w pożywce płynnej. Kiedy pojawiały się rośliny z in vitro na sklepowych półkach akwaryści bardzo chwalili łatwość usuwania żelu z korzeni. Wyciąganie roślin z wełny mineralnej na ogół wymaga uszkodzenia sytemu korzeniowego. W przypadku roślin z żelu nie ma tego problemu. Z czasem jednak akwaryści zaczęli szukać jeszcze wygodniejszych rozwiązań i pojawił się kubeczek z roślinami z in vitro, w którym nie było już żelu ale ciecz. Ta ciecz to nic innego jak sterylna pożywka płynna, która zawiera wszystkie substancje odżywcze ale nie zawiera agaru. Do żelowania pożywek możemy użyć różnych substancji. Obecna technologia daje możliwość użycia szeregu syntetycznych, bądź naturalnych środków żelujących. Naturalnym, najbardziej powszechnym środkiem żelującym jest agar. Pozyskiwany jest z morskich krasnorostów. Popularnymi syntetycznymi zamiennikami są Gelrite, czy Phytagel. Produkowane są one przy użyciu bakterii i cechują się szybszym procesem zestalania oraz dodaje się ich znacznie mniej na jednostkę objętości niż agaru. Są zatem wydajniejsze i dzięki nim można uzyskać zupełnie transparentny żel.
W większości przypadków do pożywek dodaje się również regulatory wzrostu, czyli hormony roślinne. Najczęściej są to auksyny (kwas indolilo-3-octowy –IAA; kwas indolilo-3-masłowy- IBA; kwas 2,4-dichlorofenoksyoctowy- 2,4-D), cytokininy (kinetyna – Kin; 6- benzylaminopuryna – BAP) oraz gibereliny (kwas giberelinowy- GA3). Każda grupa hormonów odpowiada za odmienne procesy. Znając najczęstsze efekty powodowane użyciem danej grupy hormonów można projektować skład pożywki w celu uzyskania specyficznej reakcji rośliny. Pewne hormony odpowiadają za wytwarzanie nowych pędów i ich wydłużanie, inne za ukorzenianie. Powinno dobierać się takie proporcje hormonów, aby zapewnić najszybszy i najbardziej wydajny wzrost pędów.
Pożywka powinna mieć też odpowiednie pH. Dobiera się zazwyczaj lekko kwaśne. W takim pH lepiej rozpuszczają się sole oraz obserwuje się lepszy wzrost roślin. Przygotowana mieszanina soli, hormonów oraz innych dodatków musi zostać wysterylizowana. Sterylizacja odbywa się w autoklawie. W przypadku składników termolabilnych niezbędne jest dodanie ich już po autoklawowaniu. Przykładem takich substancji są antybiotyki służące do walki z zakażeniami w kulturach. Zostają one dodane w komorze laminarnej. W takich właśnie komorach prowadzi się pracę z kulturami. Jest to maszyna zawierająca przestrzeń, przez którą przepływa filtrowane powietrze. Odpowiedni system filtracji daje gwarancję, że powietrze w komorze nie zawiera komórek bakterii, grzybów, a nawet w bardziej wydajnych filtrach wirusów. Komory mogą być dzielone ze względu na sposób przepływu powietrza, na komory z pionowym lub poziomym przepływem powietrza.
Do pracy w komorze potrzebne jest kilka podstawowych narzędzi. Oprócz zestawu pincet oraz skalpeli używanych do bezpośredniego kontaktu z tkanką potrzebny jest przyrząd do sterylizacji narzędzi – palnik (opala się narzędzia w stożku ognia. Tam temperatura jest największa i osiągana przeszło 600st. C) lub sterylizator kulkowy (sterylizacja kilka minut w temperaturze >200 st. C), naczynie na zlewki płynu pokulturowego, bądź odpady stałe, sterylne szalki Petriego, na których układa się materiał roślinny.
Mikrorozmnażanie można prowadzić różnymi technikami – za pomocą regeneracji bezpośredniej, pośredniej lub somatycznej embriogenezy (choć niektórzy nie uznają jej za metodę mikropropagacji). Regeneracja bezpośrednia polega na odtworzeniu organu rośliny bezpośrednio z tkanki, bez udziału tkanki przyrannej (kallusa). Jako eksplantat najczęściej wykorzystuje się uśpione pąki boczne. Dzięki działaniu cytokinin, bądź cytokinin i auksyn jednocześnie, komórki pąka bocznego zmuszane są do podziałów, co w rezultacie skutkuje powstaniem pędów. W zależności od zastosowanych hormonów może rozwinąć się od jednego pędu, tak jak dzieje się to w naturze, do nawet kilkudziesięciu. Na jednej roślinie znajduje się co najmniej jeden węzeł zawierający pąki boczne. Używając kilku węzłów jednej rośliny i posiadając zoptymalizowaną metodykę mikrorozmnażania możemy z jednej rośliny uzyskać kilkaset nowych. Należy jednak liczyć się z tym, że im więcej pędów otrzymujemy z jednego pąka bocznego, tym większe ryzyko wystąpienia zmienności somaklonalnej, opisanej w dalszej części artykułu.
Przy mikrorozmnażaniu bezpośrednim wykorzystuje się też pąki wierzchołkowe. Wycina się fragment rośliny o długości od kilku milimetrów do kilku centymetrów zawierający taki pąk, a następnie umieszcza w pożywce. W ten sposób uzyskujemy z jednego pąka jedną roślinę. Metoda ta jest mało efektywna, ale ma swoje zalety. Dzięki niej można wyeliminować z rośliny wirusy. Wycinając odpowiednio mały fragment pąka (mniejszy niż 1mm) jest szansa na to, że jego komórki będą wolne od wirusów. Następnie tak powielana roślina jest w 100% zdrowa. Bardzo ciekawym zjawiskiem jest również wykształcanie pędów przybyszowych bezpośrednio z tkanki liści czy łodyg. Takie pędy można bardzo łatwo ukorzenić, a następnie użyć jako sadzonki.


Eksplantaty można zmusić również do produkcji tkanki przyrannej – kallusa. Komórki odróżnicowują się w komórki kallusa, następnie intensywnie proliferują (namnażają się), by w końcowym etapie wytworzyć pędy. Jest to mikrorozmnażanie pośrednie, ponieważ pojawia się faza tkanki kallusowej. We wcześniej opisanych metodach nie występowała. Moim zdaniem jest to metoda warta uwagi. Z małej grudki kallusa można wytworzyć od kilkunastu do kilkudziesięciu pędów. Mankamentem jest jednak występowanie zmienności somaklonalnej podczas regeneracji. Trzeba dodatkowo przeprowadzić selekcję fenotypów, które nas interesują – tych, które są identyczne z rośliną mateczną. Uzyskane zmienione pędy należy odrzucić, a zostawić prawidłowe.
Somatyczna embriogeneza polega na powstawaniu zarodków z komórek somatycznych (z komórek wegetatywnych rośliny), a nie z komórki plemnikowej i jajowej. Tutaj również możemy zastosować podział na pośrednią i bezpośrednią somatyczną embriogenezą. Pośrednia wymaga wytworzenia kallusa embriogenicznego, natomiast bezpośrednia tworzy zarodki prosto z tkanki. Powstałe zarodki z komórek somatycznych przechodzą podobne fazy rozwojowe, które przechodzą zarodki zygotyczne. Istnieje jednak kilka ważnych różnic. U zarodków somatycznych stadium globularne jest większe niż u zarodków zygotycznych i nie wykształca się suspensor. Suspensor odpowiedzialny jest za syntezę hormonów oraz dostarcza substancje odżywcze. W warunkach in vitro jego rolę pełni pożywka. Co więcej nie wytwarzane jest bielmo, ani okrywa nasienna. Zarodki somatyczne różnią się także zawartością wody. Mają jej znacznie więcej niż zarodki zygotyczne, które przed przejściem w stan spoczynku muszą przejść proces odwodnienia. Zarodki somatyczne mogą mieć także zmienioną liczbę oraz morfologię liścieni. Somatyczna embriogeneza jest również bardzo wydajnym sposobem powielenia materiału roślinnego.
Przybliżę nieco temat wspomnianej wcześniej zmienności somaklonalnej. Nazwa ta wywodzi się od komórek somatycznych, czyli wegetatywnych, które stanowią materiał wyjściowy do mikorozmnażania oraz klonów, którymi są otrzymane rośliny. Teoretycznie w kulturach in vitro nie powinno obserwować się żadnej zmienności. Nie występuje przecież łączenie gamet osobników rodzicielskich, ani corssing-over w mejozie. Cechy rośliny potomnej powinny zostać zachowane. Mimo to możemy zaobserwować odchylenie od cech rośliny matecznej. Przyczyną mogą być między innymi mutacje DNA i zmiany metylacji DNA (zmienność epigenetyczna). Zmienność na poziomie metylacji jest na ogół odwracalna. Pędy, które wyrosną z pąków śpiących zmienionej rośliny z dużym prawdopodobieństwem nie będą posiadały niechcianych cech. Mutacje DNA są znacznie trwalsze. Zmienność może także wynikać z tego, iż komórki tej samej rośliny mogą być niejednorodne genetycznie. Wynika to z zaburzeń powstałych podczas podziałów komórkowych oraz replikacji DNA. Zmienia się ploidalność komórek. Podczas wprowadzania rośliny do kultury mogą się aktywować odmienne programy rozwojowe, charakterystyczne dla poszczególnych komórek. Szczególnie duża zmienność jest generowana przez kallus. Każda regeneracja pośrednia niesie ze sobą duże ryzyko uzyskania somaklonów. Na szczęście bardzo często są to odwracalne mutacje epigenetyczne.
Rośliny produkowane metodą in vitro mają także ogromną przewagę nad produkcją szklarniową. Jedną z najważniejszych zalet jest to, że w uprawie in vitro wykorzystywana jest bardzo mała ilość wody. Do uzyskania od kilkudziesięciu do kilkuset sadzonek wystarczy jej zaledwie 100 ml. Natomiast w szklarniach zużycie wody jest nieporównywalnie wyższe. Sterylność zachowana w produkcji in vitro, czyli brak mikroorganizmów umożliwia całkowite przyswojenie podanych substancji odżywczych wyłącznie przez rośliny. Nie korzystają z nich żadne inne organizmy, w tym glony, jak to się dzieje w szklarniach. Oszczędność mikro- i makroelementów jest ogromna. Odbija się to na bardzo korzystnej relacji ceny do ilości roślin w porcji in vitro. Kolejnym atutem uprawy roślin in vitro jest oszczędność powierzchni. Szklarnie wykorzystują tylko jeden poziom do uprawy roślin. W laboratoriach rośliny rosną na półkach z oświetleniem. Im więcej półek tym większa powierzchnia jest zaoszczędzona. Technologia In vitro wciąż się rozwija i dzięki szeregowi zalet stanowi podstawę produkcji roślinnej na świecie.
Autor: Mariusz Pożoga



